1. Características
2. Síntesis / degradación
3. Distribución
4. Función
5. Usos terapéuticos
El ácido hialurónico es un glicosaminoglicano, un polisacárido, no sulfatado de alto peso molecular que se encuentra en la matriz extracelular de todos los tejidos animales, siendo especialmente abundante en los tejidos conectivos, pero también en el tejido nervioso y epitelios. Fue aislado en 1934 del humor vítreo del ojo bovino. Es una molécula extremadamente larga con una gran capacidad de hidratación que aporta a los tejidos resistencia a presiones mecánicas y lubricación, pero también otras funciones relacionadas con la comunicación y diferenciación celular. Aunque se asocia con otras moléculas en la matriz extracelular no forma enlaces covalentes con ellas, lo que es una característica única entre los glicosaminoglicanos. Apareció tarde en la evolución, quizá a partir de los primeros animales cordados.
1. Características moleculares
La estructura molecular del ácido hialurónico fue desentrañada en 1950. Es un polímero formado por pares de disacáridos, D-glucurónico y N-acetil glucosamina, unidos mediante enlaces alternos: (1-3)-beta-D-N-acetil glucosamina- (1-4)-beta-D-glucurónico (Figura 1). Algunas moléculas pueden llegar a tener hasta 25000 repeticiones de dichas parejas y alcanzar los 20000 Da. En condiciones acuosas adopta una organización plegada y globular, pero si se extendiese tirando de sus dos extremos podría llegar a medir unas 15 µm de longitud, mayor que el diámetro de un eritrocito.

El ácido hialurónico se encuentra disuelto en la matriz en forma de sal, como hialuronato. En 1972 se descubrió que el ácido hialurónico es capaz de actuar como una especie de esqueleto central al que se asocian mediante uniones electrostáticas algunos proteoglicanos, como el agrecano, versican y neurocan, mediante interacciones electrostáticas. Actúa como el esqueleto de un andamiaje donde se pueden unir dichos proteoglicanos. Con ello se crean redes de sacáridos enormes en la matriz extracelular. Al contrario que otros glicosaminoglicanos, el ácido hialurónico no se une directamente mediante enlaces químicos covalentes a polipéptidos de la matriz extracelular, por tanto no forma proteoglicanos.
El ácido hialurónico tiene una gran capacidad de hidratación, es decir, de asociarse a moléculas de agua, puesto que posee muchas cargas negativas en su estructura molecular. Debido a su tamaño, a un pobre plegamiento de su estructura molecular (Figura 2) y a su capacidad para unir agua, puede crear un gran espacio acuoso en su interior. La proporción de agua asociada a su estructura puede ser 1000 veces mayor que su propio peso molecular. Esto favorece la difusión de moléculas no muy voluminosas a través del espacio que crea. Sin embargo, otras moléculas de mayor volumen como algunas proteínas quedarían excluidas. Aún así, su estructura cambia constantemente de organización, con lo que la posibilidad de difusión a su través es variable.

2. Síntesis y degradación
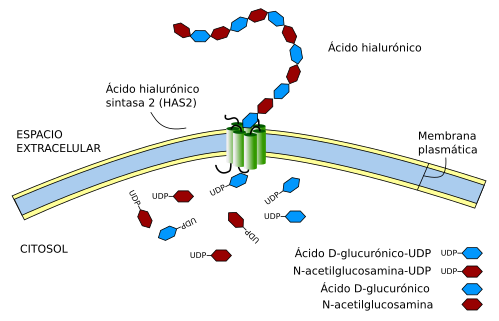
Al contrario que el resto de los glicosaminoglicanos, el ácido hialurónico se sintetiza en la membrana plasmática en vez de en el aparato de Golgi. Se sintetiza gracias a unas enzimas de membrana denominadas sintasas del ácido hialurónico, de las que hay tres tipos en vertebrados (HAS1, HAS2, y HAS3) y las cuales se expresan de forma diferencial en diferentes tejidos. La síntesis ocurre en la cara citosólica de la membrana plasmática donde se van ensamblando los monosacáridos, y a medida que se va sintetizando la cadena de ácido hialurónico va siendo transferida al espacio extracelular (Figura 3). Aunque las tres enzimas sintetizan ácido hialurónico, cada una puede sintetizar cadenas de distinta longitud, lo que unido a su expresión diferencial contribuye a que cada tejido puede tener un conjunto de moléculas de ácido hialurónico de distinto tamaño, afectando a sus propiedades. La HAS2 es la que parece sintetizar las cadenas más largas. Curiosamente un gen homólogo al de la enzima HAS1 se ha encontrado también en algunas bacterias, las cuales sintetizan ácido hialurónico para aumentar su movilidad. Probablemente estas bacterias captaron el gen de los animales.
El metabolismo del ácido hialurónico es muy dinámico. La vida de las moléculas de ácido hialurónico puede variar entre 1 y varios días. Aproximadamente 1/3 se reemplaza cada día. Se degrada por varios tipos de enzimas: hialuronidasa, beta-D glucuronidasa, beta-D-N-acetil-hexosaminidasa. Las más importantes son las hialuronidasas. También se puede degradar en los lisosomas tras endocitosis mediada por receptor. En aquellos tejidos que están bien drenados por vasos linfáticos se suele eliminar ácido hialurónico en la linfa, desde donde pasa a la sangre y es degradado fundamentalmente por las células endoteliales de los capilares sinusoidales del hígado. Aproximadamente el 30 % del ácido hialurónico que se elimina lo hace en el hígado. Una parte del ácido hialurónico también se elimina en los propios nódulos linfáticos o es excretado (1 % del ácido hialurónico corporal) diariamente por los riñones.
3. Distribución
El ácido hialurónico es el más abundante de todos los glicosaminoglicanos. En el ratón se ha encontrado que aproximadamente la mitad del ácido hialurónico se encuentra en la piel (con una concentración de 0.5mg/g) y un 25 % en los huesos y articulaciones. El resto se distribuye entre los músculos y las vísceras. Las zonas donde está más concentrado son en el cordón umbilical, en el líquido sinovial (3-4 mg/ml), humor vítreo del ojo (0.1 mg /ml) y en el folículo ovárico previo a la ovulación. Es un componente importante del líquido sinovial de las articulaciones, donde aumenta la viscosidad del fluido, y en el cartílago articular. Las menores concentraciones se encuentran en el hígado y en el suero sanguíneo. Es también un componente importante en el tejido nervioso. En el cartílago, aunque no es el glicosaminoglicano más abundante, ayuda a la estabilización de los proteoglicanos de la matriz, fundamentalmente el agrecano, donde forman agregados enormes que se disponen entre las fibras de colágeno.
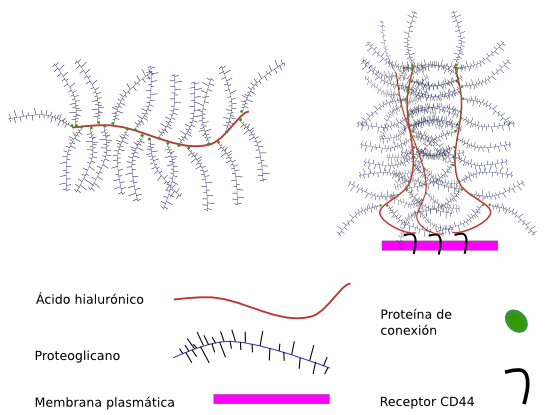
A veces el ácido hialurónico se concentra en torno a las células. Las células tienen receptores en sus membranas que pueden unirse al ácido hialurónico: CD44, HARE, LYVE-1, CD168, y el layilin. Por ejemplo, CD44 que pueden unir ácido hialurónico, quedando este en la periferia celular (Figura 4). A veces se puede detectar en el interior de las propias células.
4. Función
Las funciones que lleva a cabo el ácido hialurónico están relacionadas con sus características moleculares. Debido a su capacidad para unir agua es un excelente lubricante y aporta una gran resistencia a presiones mecánicas, pero también esta propiedad le capacita para regular el balance hídrico de los tejidos y su osmolaridad. El ácido hialurónico ayuda a crear la trama de la matriz extracelular mediante sus interacciones con los proteoglicanos o el colágeno. Cuando está muy concentrado puede interaccionar consigo mismo creando mallas o entramados que le aportan al tejido unas propiedades visco-elásticas particulares.
Las células tienen receptores específicos para el ácido hialurónico. Así, más allá de sus propiedades mecánicas e hídricas, se le ha implicado como señal molecular en la regulación de la proliferación, diferenciación y migración celular. El más importante es el CD44, que se expresa en la mayoría de las células.
La degradación del ácido hialurónico permite la permeabilización de la matriz extracelular, favoreciendo el trasiego de células. Curiosamente, los restos resultantes de la degradación del ácido hialurónico tienen carácter angiogénico e inflamatorio. Una alta concentración de ácido hialurónico en la matriz extracelular favorece la estabilidad celular e integridad tisular, mientras que la degradación favorece procesos de remodelación tisular. La estabilidad del ácido hialurónico es un indicio de madurez del tejido.
El ácido hialurónico es una buena herramienta en biotecnología y medicina, sobre todo en los procesos de reparación tisular y como armazón en cultivos tisulares. A esto ayuda que no es una molécula antigénica, es decir, no desencadena respuestas inmunes cuando se inocula en los tejidos. Por ejemplo, su primera aplicación médica fue en oftalmología donde se usó en inyecciones para mantener las formas de las cavidades oculares y como sustituto del humor vítreo. En la reparación de tejidos se sintetizan grandes cantidades de ácido hialurónico y por ello se usa en medicina para curar heridas. En la artritis se puede inyectar directamente, también en la reparación de heridas, en cirugía de operaciones estéticas, etc. También se usa para la coadministración de fármacos.
Por otra parte se ha demostrado que su presencia es importante en los nichos de las células madre, donde estimula y favorece la migración celular mediante la creación de espacios físicos para que las células se desplacen. Durante el desarrollo ayuda a la morfogénesis de estructuras embrionarias. Por ejemplo, se puede liberar desde la parte basal de los epitelios y producir la curvatura en éstos, debido a la gran cantidad de agua que atrae. Pero además favorece que los espacios intercelulares sean más transitables por las células. Por ejemplo, este proceso parece implicado en la formación embrionaria de las válvulas del corazón.
En los cultivos celulares se detecta un halo de ácido hialurónico a su alrededor de las células, secretado por ellas mismas. El papel de este halo no está claro pero parece tener dos funciones: favorecer la movilidad de la propia célula y la de protección. Este papel de protección es debido a que otras células, virus o moléculas grandes no pueden atravesar dicho halo.
5. Usos terapéuticos
El ácido hialurónico se utiliza en la industria por sus propiedades: biocompatibilidad, no inmunogénico, no inflamatorio, no tóxico. En medicina es frecuente en la cirugía de ojos, visco-suplementación en artritis, dosificación de fármacos, como lubricante en forma de hidrogeles en la implantación de biomateriales. También se usa en cosmética. Actualmente se está modificando molecularmente el ácido hialurónico y uniéndolo a otras moléculas para que sea mejor herramienta en los diferentes tratamientos.
El ácido hialurónico en sí mismo puede ser usado como una herramienta terapéutica en función de su tamaño. Así, las moléculas con alto peso molecular (>5MDa) tienen efectos antiangiogénicos e immunosupresores; con tamaños medios (20KDa-1MDa) están asociados con procesos embriológicos, con la reparación de heridas, y la regeneración; y los tamaños pequeños (6 KDa-20Kda) está asociados con fenómenos pro-inflamatorios, angiogénesis, procesos de expresión génica. Las cadenas cortas ácido hialurónico tienen efectos anti-apoptóticos e inducen la expresión de proteínas de choque térmico.
Como lubricante se puede usar en la enfermedad del ojo seco, donde se aplican lentes de contacto artificiales al ojo que van liberando ácido hialurónico de manera continuada. También en las articulaciones, en vez de hacer inyecciones repetidas se puede introducir un hidrogel que vaya liberando ácido hialurónico a lo largo del tiempo.
El ácido hialurónico se puede emplear para encapsular proteínas y mantenerlas activas para su liberación en el organismo. Es decir, se puede emplear como vector de dosis de fármacos como antibióticos y antisépticos.
Bibliografía
Bayer IS. 2020. Hyaluronic Acid and Controlled Release: A Review. Molecules 25, 2649.
Csoka AB, Stern R. 2013. Hypotheses on the evolution of hyaluronan: a highly ironic acid. Glycobiology 23:398-411.
Escudero D. 2009. HAS2 (hyaluronan synthase 2). Atlas of genetics and cytogenetics in oncology and Haematology.
Fraser JRE, Laurent TC, Laurent UBG. 1997. Hyaluronan: its nature, distribution, functions and turnover. Journal of internal medicine 242:27-33.
Laurent TC, Fraser JR. 1992. Hyaluronan. 1992. The FASEB Journal 6:2397-2404.
Necas J, Bartosikova L, Brauner P, Kolar J. Hyaluronic acid (hyaluronan): a review. 2008. Veterinarni Medicina 53:397-411.
