1. Fibronectinas
2. Lamininas
3. Matricelulares
- Tenascina
- Osteopontina
- Fibulina
4. Metaloproteinasas
Hay tres tipos de uniones que dan cohesión a los tejidos animales: uniones entre moléculas de la matriz extracelular, uniones entre las células y la matriz extracelular, y uniones entre células contiguas. La matriz extracelular es un entramado molecular cohesionado en sí misma y las moléculas que favorecen esta propiedad son principlamente glicoproteínas presentes en la propia matriz. Estas glicoproteínas establecen puentes entre las moléculas estructurales de la matriz extracelular, y entre ellas y las células. Tienen múltiples dominios de unión que reconocen y unen una gran variedad de moléculas, lo que les permite formar entramados. Entre estas glicoproteínas destacan las fibronectinas, las lamininas y las tenascinas. Aunque la cohesión mecánica es una de sus principales funciones, las glicoproteínas desempeñan también otras funciones.
1. Fibronectina
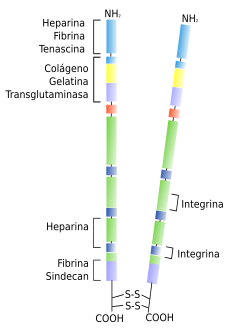
Las fibronectinas son glicoproteínas formadas por dos cadenas de polipéptidos unidos por uniones disulfuro (Figura 1). Son unas de las principales responsables de trabar la matriz extracelular. Poseen dominios en su estructura molecular que les permiten unirse al colágeno, a ciertos proteoglicanos, a glicosaminoglicanos, a la fibrina, a la heparina y a proteínas de la membrana plasmática de las células como las integrinas. Por tanto establecen uniones entre moléculas de la matriz extracelular y también entre moléculas de la matriz extracelular con moléculas celulares. Una vez liberadas a la matriz extracelular pueden interactuar entre sí para formar largas fibras en torno a la célula. Las moléculas de fibronectina se encuentran en prácticamente todos los tejidos y pueden aparecer formando fibras insolubles en los tejidos conectivos o solubles en el plasma de los fluidos corporales, como la sangre. Tienen un papel muy importante durante el desarrollo embrionario creando sendas por las que pueden migrar las células de un lugar a otro del embrión, y también son abundantes en tejidos durante los procesos de remodelación.
2. Laminina
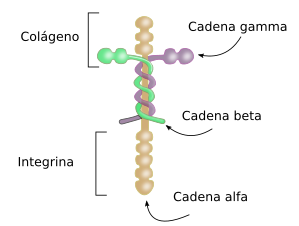
Las lamininas son uno de los principales componentes de la lámina basal, la matriz extracelular que separa a los epitelios y células musculares de los tejidos conectivos. Su estructura molecular está formada por tres cadenas de aminoácidos altamente glicosidadas unidas por puentes disulfuro (Figura 2). Estas cadenas son alfa, beta y gamma. Existen 5 tipos de cadenas alfa, 3 beta y 3 gamma, las cuales se combinan entre sí para formar diferentes tipos de lamininas, aunque no todas las combinaciones son posibles ya que se han aislado sólo 16 formas de laminina en humanos. La laminina es sintetizada por células epiteliales, musculares, neuronas y células de la médula ósea. Epitelio y células musculares depositan la laminina principalmente en las láminas basales. Aparte de su función estructural las lamininas afectan a la diferenciación y comportamiento celular gracias a que son reconocidas por las integrinas. Por ello, defectos en las lamininas suelen conllevar procesos patológicos. Son de las primeras glicoproteínas de la matriz extracelular que aparecen en el embrión.
3. Glicoproteínas matricelulares
En torno a los años 90 del siglo pasado se comprobó que algunas proteínas de la matriz extracelular producían pérdida de adhesión de las células más que aumentarla. Son proteínas que, aunque tienen lugares de reconocimiento para el colágeno, fibronectina y receptores celulares de superficie, su función no es eminentemente estructural. Estas glicoproteínas se caracterizan por ser secretadas de forma específica, temporal y espacialmente por una gran diversidad de células. Es decir, son proteínas temporales más que constitutivas en la matriz extracelular.
La función principal de las proteínas matricelulares es modificar la actividad celular y favorecer la remodelación de la matrix extracelular. Son capaces de unirse a factores de crecimiento y modifican los efectos de estos factores en las células. Siempre están presentes cuando los tejidos se están remodelando y son abundantes durante el periodo embrionario o en procesos fisiológicos. Algunas de estas moléculas incluso tienen efectos en las células durante su fase intracelular, antes de ser liberadas a la matrix extracelular. Proteínas matricelulares son, por ejemplo, la tenascina, fibulina, tromboespondinam, osteopontina y la proteína SPARC.
Tenascinas
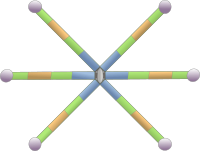
Las tenascinas forman una familia de glicoproteínas de gran tamaño con una estructura molecular haxamérica modular (Figura 3). Se producen diferentes tipos de tenascina por maduración alternativa de su ARN mensajero. La tenascina-C fue el primer tipo descubierto y se libera a la matrix extracelular de tendones, huesos y cartílago durante el desarrollo embrionario, pero también en otros tejidos del embrión. La tenascina-C no se expresa mucho en tejidos adultos pero sí cuando ocurren daños tisulares como en los infartos cardiacos. La tenascina-R abunda en el sistema nervioso, tanto durante el desarrollo como en el adulto. La tenascina-X es abundante en el tejido conectivo y se expresa mucho en músculos que tienen que hacer esfuerzos, como en los deportistas. También se han descrito las tenascinas Y y W. La tenascina-Y es el equivalente aviar de la tenascina-X. Como otras glicoproteínas, la tenascina cambia la cohesión de la matriz extracelular puesto que puede establecer enlaces con integrinas, fibronectinas, colágeno y proteoglicanos. En condiciones normales, cada tipo de tenascina se expresa en lugares concretos del organismos, que pueden cambiar según el estado de desarrollo, pero también pueden inducirse cuando hay reparación de tejidos, durante procesos tumorales o patológicos.
Osteopontina
La osteopontina está presente en el hueso, relacionada con la mineralización y remodelación ósea, y en el riñón. En menos concentración aparece en el cartílago donde reconoce a los proteoglicanos.
Fibulina
Las fibulinas son un grupo de 7 glicoproteínas secretadas en muchos tejidos y que se asocian a la lámina basal, fibras elásticas y otros componentes de la matriz extracelular. Cada fibulina se expresa de manera diferencial en diferentes del tejido y en diferentes etapas durante el desarrollo. La fibulina 5 es importante para la formación de las fibras elástica gracias a que puede unirse a la tropoelastina. Las fibulinas, además de su función en el entramado de la matriz extracelular, afectan a la fisiología de las células. Así, estas proteínas se pueden comportar tanto como matricelulares y como estructurales.
4. Metaloproteinasas. Remodelación de la matriz extracelular.
La matriz extracelular de los animales está en constante remodelación mediante la degradación de componentes y la producción de otros nuevos por parte de las células. La degradación de la matriz extracelular la llevan a cabo enzimas como las metaloproteinasas. Son enzimas que se asocian a la cara externa de la membrana plasmática (son secretadas) o forman parte integral de ella, siempre con su centro activo localizado extracelularmente. Inicialmente se producen en forma inactiva o prometaloproteinasas y para su activación es necesaria una proteolisis en su estructura, llevada a cabo por otras enzimas asociadas a la membrana plasmática. Existen unas 29 metaloproteinasas diferentes en mamíferos, cada una de las cuales tiene apetencia por distintos componentes de la matriz extracelular. Así, aunque no son totalmente específicas, se clasifican en colagenasas, gelatinasas, estromalisinas, matrilisinas, metaloproteinasas transmembrana y unidas a proteínas de membrana (Figura 4), y un grupo adicional heterogéneo. Cada grupo tiene un grupo de sustratos sobre el que tienen más apetencia. Las metaloproteinasas son capaces de degradar también receptores de membrana, proteínas de adhesión, citocinas, etcétera.

Las metaloproteinasas no sólo intervienen en el mantenimiento de la matriz extracelular sino que son cruciales en procesos como el desarrollo, remodelación de la matriz extracelular inducida por estímulos, por ejemplo, hormonas, o en procesos patológicos tales como la inflamación, reparación de tejidos o metástasis tumoral. Otro papel importante de la metaloproteinasas es liberar moléculas que se encuentran ancladas en la matriz extracelular, las cuales actúan como señal sobre las células, y que se vuelven solubles tras la degradación de la matriz extracelular. Estas enzimas no sólo son producidas por los fibroblastos sino que también las sintetizan las células epiteliales, condrocitos, osteoclastos y leucocitos, además de células malignas como las tumorales.
-
Bibliografía ↷
-
Bibliografía
Berg G, Barchuk M, Miksztowicz V. 2019. Behavior of metalloproteinases in adipose tissue, liver and arterial wall: an update of extracellular matrix remodeling. Cells 8: 158. doi:10.3390/cells8020158.
Bosman FT, Stamenkovic I. 2003. Functional structure and composition of the extracellular matrix. Journal of pathology. 200:423-428.
Halper J, Kjaer M. 2014. Basic components of connective tissues and extracellular matrix: elastin, fibrillin, fibulins, fibrinogen, fibronectin, laminin, tenascins and thrombospondins. In: Halper J. (eds) Progress in heritable soft connective tissue diseases. Advances in experimental medicine and biology, vol 802. Springer, Dordrecht
Hynes RO. 1999. Cell adhesion: old and new questions. Trends in cell biology . 9:M33-M37.
Luo BH, et al. 2007. Structural basis of integrin regulation and signaling. Annual review of immunology. 25:619-647.
Midwood KS, Chiquet M, Tucker RP, Orend G. 2016. Tenascin-C at a glance. 129: 4321-4327.
Mouw JK, Ou G, Weaver VM. 2014. Extracellular matrix assembly: a multiscale deconstruction. Nature reviews. Molecular cell biology. 15:771-785.
Murphy-Ullrich JE, Sage EH. 2014. Revisiting the matricellular concept. Matrix biology. 37:1-14.
Pankov R, Yamada KM. 2002. Fibronectin at a glance. Journal of cell science. 115:3861-3863.
-
 Glúcidos, proteoglicanos
Glúcidos, proteoglicanos 