Puede haber varias razones para evitar la inclusión de un tejido del que posteriormente obtener secciones. Durante los procesos de inclusión, como las inclusiones en parafina o en resinas tipo epoxy, se ha de someter a las muestras a deshidratación. Esto ocasiona a veces daño en algunas moléculas o regiones moleculares que son las que queremos detectar posteriormente con técnicas como la inmunohistoquímica o la hibridación in situ. Además, para observar algunas características tisulares o celulares se requieren secciones gruesas del orden de 50 µm, a veces de 100 o 200 µm. Por ejemplo, para estudiar la organización espacial de determinadas células como las neuronas es recomendable hacer cortes de un grosor superior a las 50 µm y emplear inmunohistoquímica o histoquímica para ponerlas de manifiesto. La obtención de secciones gruesas sin necesidad de inclusión se puede conseguir de dos maneras diferentes: mediante congelación de la muestra y posterior corte en un microtomo de congelación o mediante el uso del vibratomo (Figura 1).

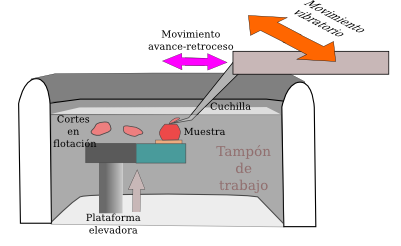
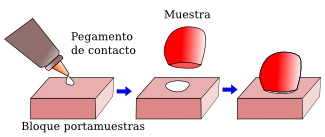
El vibratomo es un aparato con el que se obtienen secciones de un grosor que puede oscilar entre las 40-50 µm hasta varios centenares de µm partiendo de una muestra animal o vegetal endurecida sólo mediante fijación. El mecanismo de corte consiste de una plataforma sobre la que se sitúa la muestra, que puede regularse en altura y nos permite seleccionar el grosor del corte, y de una cuchilla de borde muy afilado que se desplaza horizontalmente sobre la muestra realizando el corte. La característica del vibratomo es que la cuchilla, además de avanzar sobre la muestra, posee un movimiento de vibración lateral a modo de sierra que facilita el corte y evita arrastrar el tejido (Figura 2). La muestra se encuentra adherida, normalmente mediante pegamento de contacto (Figura 3), directamente a un bloque portamuestras que se coloca sobre la plataforma elevadora.
No todas las muestras son apropiadas para ser cortadas en un vibratomo. Así, aquellas que sean muy blandas o que posean porciones demasiado duras o elásticas son normalmente arrastradas por la cuchilla, a pesar de que disminuyamos la velocidad de avance y aumentemos la oscilación de la cuchilla. Es decir, la muestra ha de tener una cierta consistencia y no poseer elementos distorsionadores del corte.
Otra característica del vibratomo es que todo el proceso de corte se realiza bajo una solución acuosa que normalmente es una solución tamponada o una solución salina (Figura 2). Para ello tanto la muestra como el borde de corte de la cuchilla han de estar sumergidos y los cortes que se obtienen se denominan cortes en flotación, es decir, no sujetos a ningún soporte. Estos cortes se pueden procesar de esta manera, flotando, o adherirse a un portaobjetos y procesarlos después. Sin embargo, el proceso de secado necesario para la adhesión al portaobjetos suele conllevar alteraciones de la calidad del tejido. Así, los cortes se suelen procesar durante toda la técnica en flotación y posteriormente se montan sobre portaobjetos para su observación con el microscopio óptico.
Hay que tener en cuenta que los cortes de vibratomo son muy gruesos y están en muy buenas condiciones de preservación. Si se quieren detectar moléculas en zonas profundas de la sección normalmente se procede a una permeabilización del tejido. Esto suele hacerse con detergentes como el Tween-20 o el Triton-X100, o con congelaciones rápidas a muy bajas temperaturas cuando queremos preservar las membranas.
 Microtomo de parafina
Microtomo de parafina 