Índice de la página
1. Formación de vesículas
- Nucleación
- Cargas
- Plegamiento
- Escisión
2. Viaje
3. Fusión de vesículas
- Anclaje
- Atraque y fusión
Las células eucariotas se caracterizan por el reparto ordenado y dirigido de moléculas entre sus diferentes compartimentos mediado por vesículas. Las vesículas son pequeños compartimentos delimitados por una membrana que transportan moléculas solubles y moléculas de membrana, que viajan en su interior o formando parte de la propia membrana de la vesícula, respectivamente.
El transporte vesicular supone una gran ventaja puesto que se puede seleccionar qué moléculas deben transportarse y a qué compartimento diana deben dirigirse. Pero ademas, las moléculas que llegan en las vesículas son necesarias para establecer identidad del propio compartimento y por tanto para determinar las funciones que éste puede llevar a cabo. Si no existiera especificidad en el reparto no habría compartimentos diferentes.
Las vesículas se forman en el compartimento fuente y se cargan con aquellas moléculas que deben ser transportadas. Una vez liberadas en el citosol, las vesículas son dirigidas hacia el orgánulo o compartimento diana, al cual reconocen, y con el que finalmente se fusionan. Entonces, las moléculas transportadas formarán parte del orgánulo diana y serán las responsables de su función. Sin embargo, otras moléculas sólo estarán de paso en ese compartimento y serán empaquetadas de nuevo en otras vesículas para dirigirse a otro compartimento celular. Algunas moléculas volverán desde el compatimento diana al compartimento fuente del que partieron en un transporte de reciclado. Hay que tener en cuenta que la mayoría de los compartimentos funcionan tanto como compartimento fuente como compartimento diana al mismo tiempo. Es frecuente que cuando un compartimento envía vesículas a otro, suele recibirlas también de este último. Así, la mayoría del tráfico vesicular entre dos compartimentos es bidireccional.
Lara formar una vesícula funcional se necesitan multitud de herramientas moleculares (Figura 1):
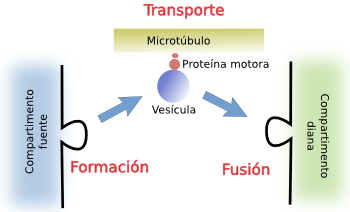
a) Moléculas para reconocer y atrapar a las moléculas que se han de transportar. Otras moléculas adicionales tienen como misión formar la vesícula a partir de las membranas del orgánulo fuente.
b) La vesícula debe conseguir proteínas para interactuar con elementos del citoesqueleto para transportar a las vesículas desde el orgánulo fuente hasta el diana.
c) Por último deben incorporar moleculas para permitir a la vesícula reconocer y fusionarse con el orgánulo diana apropiado.
1. Formación de vesículas
La formación de una vesícula en cualquier compartimento fuente es un proceso complejo (Figura 2). Participan numerosas moléculas: las que delimitan el sitio de formación de la vesícula e inician el proceso molecular, las que seleccionan a las moléculas que tienen que ser transportadas, las que participan en la formación y escisión de la propia vesícula, las que permiten posteriormente deshacerse de las proteínas de recubrimiento, etcétera.
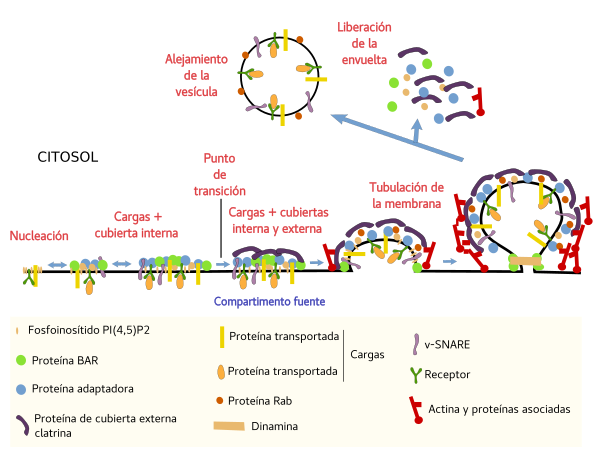
La formación de una vesícula es un proceso ordenado de reclutamiento de moléculas. En el caso de las vesículas recubiertas por clatrina, en levaduras se estima que más de 65 proteínas diferentes intervienen en el proceso formación, y en las células de mamíferos unas 50, todas ellas provenientes del citosol.
Nucleación
En las vesículas recubiertas por clatrina la nucleación se inicia mediante una concentración alta y localizada del fosfoinosítido PI(4,5)P2 en la membrana, el cual capta a las moléculas adaptadoras, que a su vez reclutará a las cargas y la cubierta de clatrina. Se ha sugerido que también concentraciones de cargas en lugares concretos de la membrana ayudarían a captar a las proteínas adaptadoras. En las vesículas COPII la nucleación se produce mediante el reclutamiento de proteínas GTPasas Sar a la membrana del orgánulo fuente. Cuando las moléculas Sar son activadas en la membrana del orgánulo fuente se encargan de reclutar a otras proteínas encargadas de seleccionar de manera específica a las cargas y a las proteínas que formarán la cubierta (Figuras 2 y 3). Hay regiones en las membranas del compartimento fuente que favorecen esta nucleación, como las zonas de transición del retículo endoplasmático.
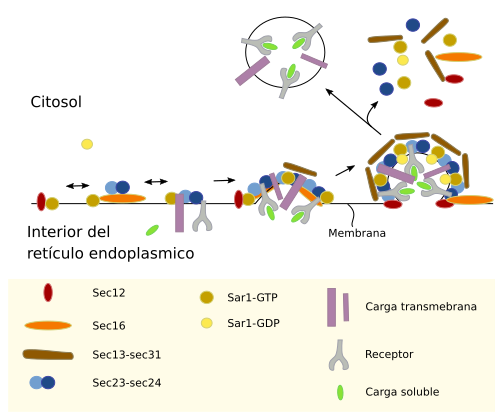
Cargas
En una vesícula se puede viajar de tres maneras: como proteína transmembrana, como ligando unido a un receptor y como molécula disuelta en el contenido de la vesícula. Las proteínas adaptadoras son capaces de reconocer secuencias señal en los dominios citosólicos de las proteínas transmembrana, algunas de ellas reconocerán a su vez a las proteínas del interior del orgánulo fuente que deben ser transportadas. Otra forma de seleccionar moléculas para incorporarlas en una vesícula es por la longitud de los dominios transmembrana de la proteína.
Plegamiento
El conjunto inicial de proteínas (GTPasas, adaptoras, cargas, etcétera) se asocian formando agregados en la membrana. Cuando se alcanza una concentración crítica se dispara el reclutamiento de otras proteínas que terminarán de formar la cubierta de la vesícula. A este momento se le llama punto de transición, y una vez alcanzado la vesícula se formará. Si no se pasa el punto de transición las moléculas que forman los agregados iniciales pueden volver a segragarse en la membrana. Aparentemente, el número de cargas que ha conseguido reunir la vesícula es importante para que termine de formarse la vesícula. Si no es suficiente la vesícula no ser formará. Entre las proteínas de la cubierta externa están aquellas que permiten entrelazar todo el entramado proteico existente, curvar la membrana y dar volumen a la vesícula incipiente, servir de centros de nucleación de actina o permitir desnudar a la vesícula de estas cubiertas tras la escisión. Cuando las proteínas de la cubierta externa superan una cantidad (para la clatrina podría ser superior al 60 % del total que formará la vesícula) es cuando la curvatura de la membrana empieza a ser visible.
Escisión
La escisión es la separación de la vesícula de la membrana madre. Curvar la membrana de una vesícula y escindirla del compartimento fuente es un proceso coordinado que requiere energía y la participación de varias proteínas. Por ejemplo, hay proteínas que ayudan a las proteínas de la cubierta externa y que se insertan en una monocapa de la membrana gracias a unas secuencias de aminoácidos denominadas BAR que son capaces de generar curvatura en diferentes momentos de la formación de la vesícula. Por ejemplo, la proteínas GTPasa Sar1 participa en la fase inicial de la curvatura. La polimerización de filamentos de actina y la acción de la miosina son también necesarios para generar fuerzas motoras que ayudan en la protusión y posteriormente en la esción de las vesículas recubiertas por clatrina. La escisión o la independencia física de la vesícula respecto al compartimento fuente requiere de curvatura, fuerza motora, pero también de otras proteínas, denominadas dinaminas, que estrangulan la comunicación membranosa entre el compartimento fuente y la vesícula. Las vesículas recubiertas por COPII no precisan ni de dinamina ni de filamentos de actina para su formación. Tras la escisión muchas de las proteínas que envuelven a la vesícula son liberadas y devueltas al citosol para realizar un nuevo ciclo con la formación de una nueva vesícula, de manera que tenemos una vesícula casi desnuda.
2. Viaje
Tras la separación del compartimento fuente se produce la eliminación de la cubierta. Hay dos mecanismos que favorecen la eliminación de las proteínas de la cubierta de la clatrina. Una la acción de chaperonas, como la HSC70, la otra es la defosforilación de PI(4,5)P2. La HSC70 se incorpora en la fase de escición de la vesícula. La liberación de la cubierta de las vesículas permite que éstas puedan interactuar con el citoesqueleto y el compartimento diana.
Tras la separación del compartimento fuente, y la liberación de la cubierta, la vesícula es dirigida hacia el compartimento diana. Este viaje está mediado por proteínas motoras y elementos del citoesqueleto, tanto filamentos de actina como microtúbulos. En las células animales los microtúbulos juegan un papel importante en el tráfico de las vesículas, aunque también participan los filamentos de actina. Sin embargo, en las plantas el tráfico vesicular está fundamentalmente mediado por los filamentos de actina.
3. Fusión de vesículas
El mecanismo de fusión de una vesícula con su compartimento diana es complejo (Figura 4). Ha de ser selectivo puesto que la célula ha de asegurarse de que una vesícula sólo se fusiona con aquel compartimento para el que las moléculas que transporta han sido destinadas. Pero además, abrir y fusionar membranas supone saltar una barrera termodinámica importante. Esto se hace en pasos sucesivos.
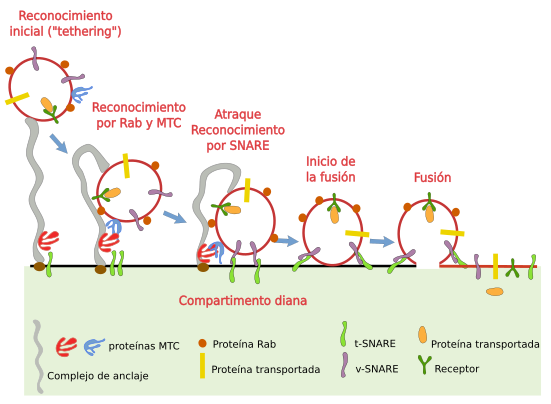
Anclaje
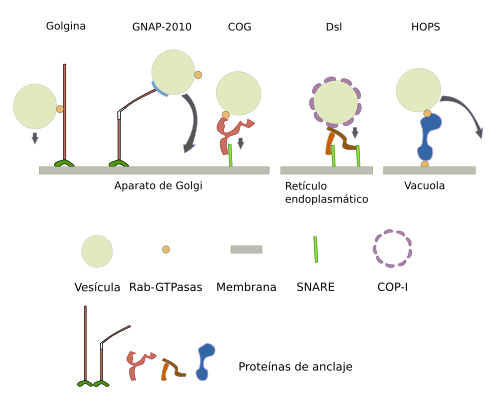
El primer paso es un reconocimiento inicial o anclaje (en inglés: "tethering"). Esto requiere que haya una especie de etiqueta a modo de código postal en la vesícula que sea reconocida por el compartimento con el que se ha de fusionar. Este reconocimiento inicial es similar al de una caña de pescar anclada en el compartimento diana que reconoce y ancla ("pesca") una vesícula que tiene unas determinadas moléculas. Las "cañas" de pescar son unos complejos proteicos asociados a las membranas del compartimento diana. Hay distintos tipos complejos: Golginas, CORVET, Dsl1, exocysto, GARP/VFT, HOPS/Class C VPS, TRAPPI y TRAPPII, que se distribuyen de forma selectiva en distintos compartimentos (Figura 5). Estos complejos pueden cambiar entre estado estirado y contraído, pudiento en algunos casos medir más de 200 nm de longitud, lo que indica que es una caña molecular bastante larga. La presencia de estas moléculas es suficiente para capturar vesículas ("tethering") y su localización diferencial en los diferentes compartimentos del Golgi (cis, medio y trans) permite seleccionar qué vesículas se capturan en cada dominio.
Atraque y fusión
El reconocimiento inicial descrito anteriormente es esencial para los pasos posteriores. Otras proteínas actúan después llamadas proteínas MTC ("multi-subunit tethering complex") que acercan aún más la membrana vesicular a la membrana del compartimento diana para que se pueda dar otro reconocimiento adicional entre otras proteínas denominadas SNARE. Son proteínas transmembrana (en humanos hay 37 diferentes) de las cuales hay dos tipos: v-SNARE y t-SNARE. Las v-SNARE se incorporan en la vesícula durante su formación en el compartimento fuente y las t-SNARE se encuentran en las membranas del compartimento diana. La interacción entre v-SNARE y t-SNARE provoca un acercamiento mucho mayor de las membranas de la vesícula y del compartimento diana, liberando además la energía necesaria para la fusión de ambas membranas. Sin embargo, para la fusión de la membrana vesicular y del compartimento fuente, otras proteínas parecen cooperar con las proteínas SNARE. Las SNARE son otra capa de especificidad en el reconocimiento del compartimiento diana por una vesícula determinada. Los filamentos de actina parecen tener un papel relevante en la fusión de las vesículas, al menos durante la secreción regulada.
Bibliografía
Borgese N. Getting membrane proteins on and off the shuttle bus between the endoplasmic reticulum and the Golgi complex. Journal of cell sciences. 2016. 129: 1537-1545.
Budnik A, Stephens EJ. ER exit sites – Localization and control of COPII vesicle formation. FEBS letters. 2009. 583: 3796–3803.
Cai H, Reinisch K, Ferro-Novick S. Coats, tethers, Rabs, and SNAREs work together to mediate the intracellular destination of a transport vesicle. Developmental cell. 2007. 12:671-682.
Kaksonen M, Roux A. Mechanisms of clathrin-mediated endocytosis. Nature reviews in mollecular cell biology. 2018. doi:10.1038/nrm.2017.132.
Kuhlee A, Raunser S, Ungermann C. Functional homologies in vesicle tethering. FEBS letters. 2015. 589:2487-2497.
Maldonado-Baez L, Wendland B. Endocytic adaptors: recruiters, coordinators and regulators. Trends in cell biology. 2006. 16:505-513.
Martens S, McMahon H T. Mechanisms of membrane fusion: disparate players and common principles. Nature reviews in molecular cell biology. 2008. 8:543-556.
Tran DT, Ten Hagen KG. Real-time insights into regulated exocytosis. Journal of cell science. 2017. 130:1355-1363.
McNiven MA, Thompson HM. Vesicle formation at the plasma membrane and trans-Golgi network: the same but different. Science. 2006. 313:1591-1594.
Weinberg J, Drubin DG. Clathrin-mediated endocytosis in budding yeast. Trends in cell biology. 2012. 22:1-13.
Witkos TM, Lowe M. Recognition and tethering of transport vesicles at the Golgi apparatus. Current opinion in cell biology. 2017. 47:16–23.
